Nel testo che segue spiegheremo perche’ si può fare e soprattutto, perché si dovrebbe?
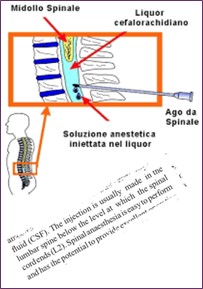
La terminazione del cono midollare è normalmente situata a livello del bordo inferiore di L1 o a livello dello spazio intervertebrale L1-L2.
Per questo motivo nell’esecuzione delle anestesie spinali subaracnoidee da sempre si raccomanda di non pungere al di sopra di L2 per evitare di incontrare il midollo.
Ma la spinale al di sotto di L2 è sempre sicura? Niente affatto. Per esempio, poichè il cono midollare è presente a livello L2 nel 43% delle donne e nel 27% degli uomini, considerato anche l’angolo di entrata dell’ago spinale la probabilità di trovare il midollo pungendo a L2-L3 varia fra 4-20%.
Le probabilità di avere il midollo a portata di ago ad un livello ritenuto sicuro aumentano se la scelta dello spazio non è fatta sulla base di un riscontro ecografico. Infatti, basandosi sulla palpazione della linea di Tuffier congiungente le creste iliache come repere a L4 o L4-L5, si cade spesso in inganno per la possibile posizione più alta della linea e/o per errori di identificazione della stessa e del conteggio degli spazi. Il risultato è che si arriva a pungere da uno a due spazi più in alto di quanto ritenuto nel 59% dei casi. Addirittura, in un gruppo di anestesisti esperti convinti di pungere a L3-L4, il livello della puntura si è rivelato essere da uno fino a quattro
spazi più in alto.
E’ quindi probabile che nella normale pratica ciascuno di noi abbia già effettuato decine se non centinaia di punture spinali a un livello considerato sicuro ma in cui in realtà il midollo era presente sulla traiettoria dell’ago.
Considerato che il livello lombare è quello in cui le strutture nervose sono più anteriorizzate e quindi più vicine alla dura, è del tutto possibile che si sia punto il midollo chissà quante volte, magari attribuendo una parestesia temporanea alla puntura di una radice piuttosto che di un cordone.
Allo stesso modo è possibile che una puntura del midollo passi del tutto inosservata non avendo interessato i fasci sensitivi e/o non avendo provocato edemi o piccole emorragie intraparenchimali.
Infatti il midollo non è così vulnerabile all’ago come si pensa.
In passato diverse procedure diagnostiche e terapeutiche venivano attuate attraversando deliberatamente il midollo con un ago sotto guida radiografica, il più delle volte senza conseguenze.
Detto questo, è ovvio che è sempre bene fare di tutto per evitare un possibile contatto fra ago e midollo anche quando la puntura è eseguita al livello lombare ritenuto “sicuro”.
Dobbiamo quindi adottare un metodo che limiti al minimo questa possibilità.
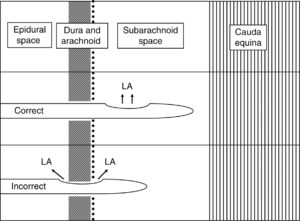
Questo metodo esiste e consiste nell’introduzione dell’ago in avanzamenti di 2mm con estrazione del mandrino e controllo del reflusso del CSF dopo ogni avanzamento (vedi video didattico/pillola) . Così facendo, è tecnicamente impossibile superare la dura ed entrare nello spazio subaracnoideo per più di 2mm.
Il click durale, non essendo sempre presente e/o percepibile, non dovrebbe essere considerato come target per l’identificazione dello spazio subaracnoideo in quanto la sua assenza spinge ad avanzare l’ago oltre misura.
Inoltre, l’uso di un ago atraumatico pencil point è paradossalmente meno sicuro di quello di un ago Quincke per due motivi.
Il primo motivo è che la punta atraumatica, a differenza della tagliente, sposta la dura prima di perforarla, creando un effetto tenting che fa avanzare inutilmente l’ago per alcuni mm durante la perforazione (fig.1).
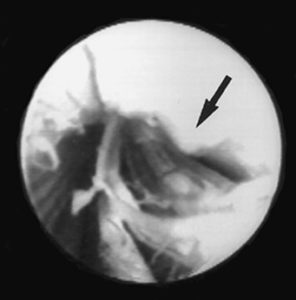
Il secondo motivo risiede nella posizione del foro dell’ago: negli aghi atraumatici si trova lateralizzato e ad una certa distanza dalla punta, originando un tratto “cieco” dell’ago di almeno 1mm che entra nello spazio prima di evidenziare il flusso di CSF, e se non considerato quest’ultimo, esso rappresenta una delle cause di possibile fallimento dell’anestesia spinale (fig.2).
Sommando le due circostanze, è quindi evidente che con l’uso degli aghi a punta tagliente si guadagnino in sicurezza almeno 3mm rispetto a quelli atraumatici.
Parlando dell’esecuzione delle anestesie spinali a livello toracico è logico che lo stesso metodo di sicurezza sia ritenuto indispensabile per la presenza certa del midollo.
Tuttavia a livello toracico l’anatomia viene in aiuto per la presenza di uno spazio disponibile fra dura e midollo variabile fra 5-8mm, di molto superiore rispetto al livello lombare dove tale spazio viene addirittura quasi annullato. (fig.3-5)
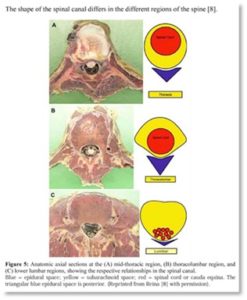
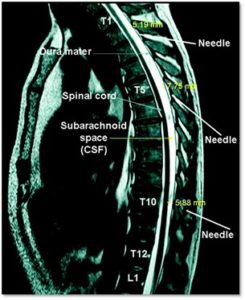
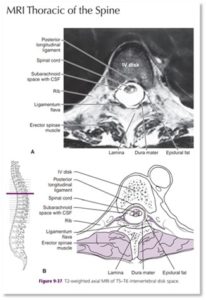
La tecnica già descritta, assicurando una penetrazione della dura non superiore ai 2mm, mette quindi al riparo da possibili inconvenienti a tutti i livelli della colonna toracica. (fig.6)
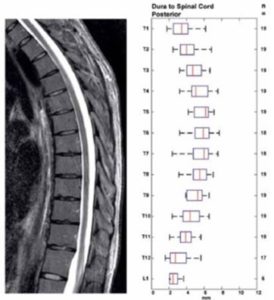
La posizione seduta a capo flesso che accentua la curvatura cifotica della colonna vertebrale aumenta la separazione posteriore del midollo spinale e della guaina durale a livello toracico e dovrebbe essere quindi preferita alla posizione sul fianco che invece la riduce. (fig.7)
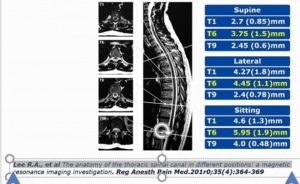
Infine, un ulteriore elemento di sicurezza è dato dall’aumento della distanza dura-midollo quando l’ago è inserito con l’inclinazione craniale resa necessaria dalla morfologia e dalla sovrapposizione dei processi spinosi toracici.
Quindi, perché pungere a livello toracico?
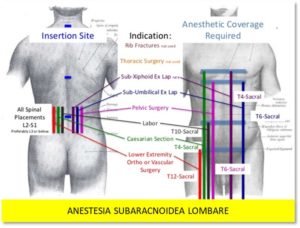
Il razionale di pungere al di sopra di L2 trova riscontro nei vantaggi apportati da una anestesia segmentale (metamerica) in tutta la chirurgia addominale e parte della toracica.
L’anestesia segmentale spinale consiste nel depositare l’anestetico direttamente al livello metamerico prescelto per ottenere la copertura viscerale e somatica richiesta dall’intervento con la minore quantità di anestetico possibile e il maggior risparmio dei distretti non interessati dalla chirurgia.
Tale metodica richiede quindi la puntura spinale al di sopra del livello L2-L3 e specificatamente a livello toracico.
Rispetto aIla puntura subaracnoidea lombare, la puntura toracica permette:
– l’esclusione di metodi empirici poco affidabili adottati per ovviare al basso livello di puntura ed estendere così lo spread cefalico del farmaco, quali l’impiego di una dose consistente di anestetico iperbarico e l’utilizzo della gravita’ tramite il posizionamento del paziente in Trendelemburg.
– il blocco segmentale selettivo con una minor quantità di anestetico, risparmio dei distretti non coinvolti dalla chirurgia e conseguente assenza di effetti collaterali quali il blocco motorio e il pooling ematico a livello degli arti inferiori e il coinvolgimento della funzione vescicale. (fig. 8-9)
Fig.8 – Si evidenzia l’estensione del blocco agli arti inferiori per la chirurgia addominale e pelvica quando il livello di puntura è al di sotto di L2.
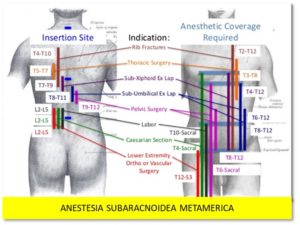
Fig.9 – Si evidenzia l’estensione del blocco limitata a T12-L1 quando il livello di puntura è a livello toracico.
Lo sviluppo delle tecniche neurassiali con approccio toracico ha reso possibile l’esecuzione “da svegli” di tipologie di intervento finora ritenute esclusivamente fattibili in anestesia generale, sia per distretti coinvolti che per tecnica chirurgica adottata, come quella laparoscopica o robotica.
I noti vantaggi della conduzione in neurassiale dei pazienti critici possono quindi essere estesi a tutta la chirurgia addomino-pelvica.
L’aggiunta del catetere subaracnoideo toracico permette di titolare una già ridotta dose di anestetico in ulteriori piccole dosi incrementali di cui e’ possibile verificare l’effetto in tempo reale, così da usare la minor quantità possibile in assoluto di farmaco e limitarne gli effetti collaterali.
Il catetere permette inoltre di estendere il blocco per la durata richiesta dalla chirurgia e può essere usato per l’analgesia, per cui la singola procedura spinale sostituisce a tutti gli effetti le più comuni procedure combinata peri-sub e peridurale ottimizzandone i risultati.
La tecnica di posizionamento del catetere intratecale non è sostanzialmente differente da quella di un catetere epidurale. Una volta raggiunto con l’ago lo spazio subaracnoideo, il catetere viene introdotto per una lunghezza massima di 4-5cm.
Dato il piccolo calibro del catetere, esso deve essere maneggiato facendo molta attenzione a non causare piegamenti ed angolature.
La comparsa di parestesie transitorie durante l’inserimento è piuttosto frequente (20-25%) e non porta conseguenze.
Un eventuale ostacolo alla progressione del catetere avviene di solito in corrispondenza della punta dell’ago. In questo caso può trattarsi di un incompleto passaggio del foro attraverso la dura, sufficiente per permettere il reflusso di CSF ma non il passaggio del catetere.
In questi casi, se si è utilizzata la tecnica corretta, si può risolvere estraendo il catetere e avanzando ulteriormente l’ago di 1mm. Dopo controllo del reflusso di CSF si può tentare una nuova introduzione. Il corretto posizionamento del catetere è confermato dal reflusso del CSF che può essere spontaneo o provocato tramite aspirazione attraverso il connettore Fissaggio e medicazione del catetere sono gli stessi dei cateteri epidurali.
BIBLIOGRAFIA
– Thomson A. Fifth annual report of the committee of collective investigation of the Anatomical Society of Great Britain and Ireland for the year 1893–94. Journal of Anatomy and Physiology 1894; 29: 35–60.
– Reynolds F. Damage to the conus medullaris following spinal anaesthesia. Anaesthesia. 2001 Mar;56(3):238-47. doi: 10.1046/j.1365-2044.2001.01422-2.x. PMID: 11251431.
– Van Gessel EF, Forster A & Gamulin Z. Continuous spinal anesthesia: where do spinal catheters go? Anesthesia and Analgesia 1993; 76: 1004–7.
– Broadbent, C.R., Maxwell, W.B., Ferrie, R., Wilson, D.J., Gawne-Cain, M. and Russell, R. (2000), Ability of anaesthetists to identify a marked lumbar interspace. Anaesthesia, 55: 1122-1126. https://doi.org/10.1046/j.1365-2044.2000.01547-4.x
– Heinz ER, Goldman RL. The role of gas myelography in neuroradiologic diagnosis. Comments on a new and simple technique. Radiology. 1972 Mar;102(3):629-34. doi: 10.1148/102.3.629. PMID: 5060173.
– Tampieri D, Melanson D, Ethier R: Spinal cord puncture: Diagnostic and therapeutic aspects, Imaging of Brain Metabolism: Spine and Cord Interventional Neuroradiology. Edited by Nadjmi M. New York, Springer-Verlag, 1989, pp 197–200
– Quencer RM: Needle aspiration of intramedullary and intradural extramedullary masses of the spinal cord. Radiology 1980;134: 115–126
– Imbelloni LE, Gouveia MA (2016) Thoracic Spinal Anesthesia. J Anesth Crit Care Open Access 4(5): 00160.
– Shatri G, Singh A. Thoracic Segmental Spinal Anesthesia. [Updated 2022 Jan 25]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2022 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK572087/
– Roupen Hatzakorzian, Ross Robbins, Gilles Plourde; Spinal Anesthesia at the Cervicothoracic Level. Anesthesiology 2001; 95:266–268 doi: https://doi.org/10.1097/00000542-200107000-00041
– Lee RA, van Zundert AA, Botha CP, Lataster LM, van Zundert TC, van der Ham WG, Wieringa PA. The anatomy of the thoracic spinal canal in different postures: a magnetic resonance imaging investigation. Reg Anesth Pain Med. 2010 Jul-Aug;35(4):364-9.
– Soltan WA, Fathy E, Khattab M, Mostafa MS, Hasan H, Refaat A, Eltantawy MAM, Ziada HFM, Sarhan MD. Combined Thoracic Spinal-Epidural Anesthesia for Laparoscopic Sleeve Gastrectomy; One Hundred Case Experience. Obes Surg. 2022 Feb;32(2):457-462. doi: 10.1007/s11695-021-05796-x. Epub 2022 Jan 4. PMID: 34981323.
– Santoro E, Colace L, Pedullà G, Pullano C. Spinal and Epidural Anesthesia for Laparoscopic Abdominal Surgery: 84 Procedures. World J Surg Surgical Res. 2021; 4: 1334
– Vincenzi P, Stronati M, Isidori P, Iuorio S, Gaudenzi D, Boccoli G, Starnari R. Opioid-Free Segmental Thoracic Spinal Anesthesia with Intrathecal Sedation for Breast and Axillary Surgery: Report of Four Cases. Local Reg Anesth. 2022 May 9;15:23-29.
– Castellani D, Starnari R, Faloia L, Stronati M, Venezia A, Gasparri L, Claudini R, Branchi A, Giampieri M, Dellabella M. Radical cystectomy in frail octogenarians in thoracic continuous spinal anesthesia and analgesia: a pilot study. Ther Adv Urol. 2018 Sep 3;10(11):343-349.
– Spannella F, Giulietti F, Damiani E, Faloia L, Stronati M, Venezia A, Vincenzi P, Castellani D, Boccoli G, Dellabella M, Giampieri M, Sarzani R, Starnari R. Thoracic continuous spinal anesthesia for high-risk comorbid older patients undergoing major abdominal surgery: one-year experience of an Italian geriatric hospital. Minerva Anestesiol. 2020 Mar;86(3):261-269.
– Vincenzi P, Starnari R, Faloia L, Grifoni R, Bucchianeri R, Chiodi L, Venezia A, Stronati M, Giampieri M, Montalti R, Gaudenzi D, De Pietri L, Boccoli G. Continuous thoracic spinal anesthesia with local anesthetic plus midazolam and ketamine is superior to local anesthetic plus fentanyl in major abdominal surgery. Surg Open Sci. 2020 Jul 17;2(4):5-11.
– Starnari R, Pullano C. “Fascial plane blocks and neuraxial blocks: two planets not so far apart.” Ultrasound guided nerve blocks of the trunk and abdominal wall, edited by Fusco P, Blanco R, Tran D, Marinangeli F, ESRA Publishing, 2021, 205-216